news.med.br
-
Pharma News
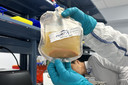
Uma pessoa recebeu pela primeira vez um tratamento experimental que, se for bem sucedido, irá levá-la a desenvolver um “fígado em miniatura” adicional, que crescerá em um linfonodo1 da própria pessoa. O procedimento, desenvolvido pela empresa de biotecnologia LyGenesis, marca o início de um ensaio clínico destinado a pessoas cujo fígado2 está falhando, mas que não receberam um transplante de órgão. Em um comunicado, a empresa anunciou que um voluntário inicial com insuficiência hepática3 recebeu uma injeção4 de células5 de doadores para transformar um de seus gânglios linfáticos6 em um segundo fígado2, mas levará meses até sabermos se o fígado2 em miniatura substitui totalmente a função hepática7.
[Mais...]
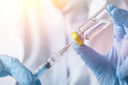
Um regime de vacina1 de três doses preveniu infecções2 pelo vírus3 da hepatite4 E (HEV) com alta eficácia em adultos ao longo de 10 anos, concluiu um ensaio de fase III da China, com resultados publicados no The Lancet. A vacina1 HEV239, vendida sob o nome Hecolin, teve uma taxa de eficácia de 83,1% na análise de intenção de tratar modificada do estudo e 86,6% em uma análise por protocolo durante esse período.
[Mais...]
Um menino de 11 anos foi a primeira pessoa nos EUA a receber uma terapia genética experimental conhecida como AK-OTOF para surdez congênita1. O tratamento foi um sucesso, segundo comunicado da empresa Akouos, subsidiária da Eli Lilly. O tratamento genético tem como alvo um tipo específico de surdez congênita1 e em breve será testado em crianças mais novas. O objetivo da terapia genética é substituir o gene mutante da otoferlina nos ouvidos dos pacientes por um gene funcional. A terapia genética desenvolvida consiste em um vírus2 inofensivo que transporta novos genes de otoferlina em duas gotas de líquido que são delicadamente injetadas ao longo da cóclea, entregando os genes a cada célula3 ciliada. Segundo o comunicado de imprensa, a restauração auditiva foi observada dentro de 30 dias após uma única administração de AK-OTOF.
[Mais...]
A FDA dos Estados Unidos aprovou o gel tópico1 de triterpenos de bétula (Filsuvez) para o tratamento da epidermólise bolhosa (EB), anunciou a Chiesi Global Rare Diseases. A aprovação estipula o uso para feridas de espessura parcial em pacientes adultos e pediátricos com pelo menos 6 meses de idade com EB distrófica e EB juncional. O apoio para a aprovação veio do ensaio internacional randomizado2 de fase III EASE, que comparou o gel de triterpenos de bétula com um gel de controle em 223 pacientes com EB, incluindo 156 pacientes pediátricos. O estudo atingiu o objetivo primário, mostrando que 41,3% dos pacientes tratados com o gel ativo alcançaram o primeiro fechamento completo da ferida alvo em 45 dias, em comparação com 28,9% do grupo controle.
[Mais...]
As empresas farmacêuticas Alnylam e Roche anunciaram que seu medicamento experimental de RNA de interferência (RNAi) que tem como alvo o angiotensinogênio reduziu a pressão arterial sistólica1 média dos pacientes. Os pacientes nos braços do zilebesiran do estudo KARDIA-1 observaram reduções na pressão arterial sistólica1 de mais de 15 mmHg 3 meses após a administração e continuaram a mostrar uma redução sustentada até 6 meses após a administração subcutânea2 do medicamento, atingindo o desfecho primário do ensaio de fase 2.
[Mais...]
Um tratamento contra o câncer1 que salva vidas pode, por si só, causar câncer1, informou a Food and Drug Administration (FDA) dos Estados Unidos em um comunicado. O tratamento, denominado CAR-T, foi aprovado pela primeira vez em novembro de 2017 para cânceres do sangue2 potencialmente fatais. Mas a FDA afirmou que recebeu 19 relatos de novos tipos de câncer1 no sangue2 em pacientes que receberam o tratamento. Dessa forma, a agência lançou uma investigação sobre o que chamou de “risco sério” de malignidades de células3 T em pacientes tratados com terapias de células3 T com receptor de antígeno4 quimérico autólogo (CAR) visando o antígeno4 de maturação de células3 B (BCMA) ou CD19.
[Mais...]
Um pequeno ensaio clínico de um tratamento para redução do colesterol1 baseado na edição genética CRISPR produziu resultados promissores. O efeito já dura seis meses desde que o primeiro participante foi tratado, e a expectativa é que seja permanente – mas um ataque cardíaco em uma pessoa levantou preocupações de segurança. As descobertas foram apresentadas nas Sessões Científicas de 2023 da American Heart Association e relatados pela Verve Therapeutics em um comunicado. Nas três pessoas com hipercolesterolemia2 familiar heterozigótica que receberam as doses mais elevadas do VERVE-101, os níveis de colesterol1 LDL3, que está ligado ao risco de doenças cardíacas, caíram entre 39 e 55 por cento.
[Mais...]
Apenas 13 anos após a descrição da técnica de edição genética CRISPR, os órgãos reguladores do Reino Unido aprovaram o “primeiro tratamento genético do mundo” em 15 de novembro, para o tratamento da doença falciforme e da talassemia1 β dependente de transfusão2. Casgevy (exagamglogene autotemcel [exa-cel]) é o primeiro medicamento que utiliza a ferramenta de edição genética CRISPR a ser licenciado para uso em pacientes. A decisão histórica poderá transformar o tratamento da doença falciforme e da talassemia1 β, mas a tecnologia é cara.
[Mais...]
Uma forma de terapia genética estabilizou ou melhorou a retinopatia diabética1 (RD) por até um ano, particularmente em pacientes com RD não proliferativa (NP), mostrou um pequeno estudo clínico, com resultados divulgados em comunicado da REGENXBIO, publicado na Cision PR Newswire. No geral, cerca de 40% dos pacientes melhoraram o estado da doença e outros 30% apresentaram doença estável após uma única injeção2 de RGX-314 direcionado ao fator de crescimento do endotélio vascular3 (VEGF). No subgrupo de pacientes com RDNP, 29 dos 30 apresentaram doença estável ou melhora na Escala de Gravidade da Retinopatia Diabética1 (DRSS), incluindo todos os pacientes tratados com a dose mais elevada.
[Mais...]
A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou em 25/09/2023 o medicamento Mounjaro (tirzepatida), fabricado pela farmacêutica Eli Lilly. O medicamento é indicado como adjuvante à dieta e exercícios para melhorar o controle glicêmico de adultos com diabetes mellitus1 tipo 2. Em ensaios clínicos2, além de reduzir efetivamente a HbA1c3, o receptor de GIP e agonista4 do receptor GLP-1 ajudou pessoas com sobrepeso5 ou obesidade6 a perder peso significativo.
[Mais...]
|