news.med.br
-
Pharma News
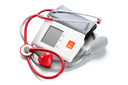
As empresas farmacêuticas Alnylam e Roche anunciaram que seu medicamento experimental de RNA de interferência (RNAi) que tem como alvo o angiotensinogênio reduziu a pressão arterial sistólica1 média dos pacientes. Os pacientes nos braços do zilebesiran do estudo KARDIA-1 observaram reduções na pressão arterial sistólica1 de mais de 15 mmHg 3 meses após a administração e continuaram a mostrar uma redução sustentada até 6 meses após a administração subcutânea2 do medicamento, atingindo o desfecho primário do ensaio de fase 2.
[Mais...]
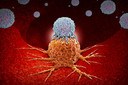
Um tratamento contra o câncer1 que salva vidas pode, por si só, causar câncer1, informou a Food and Drug Administration (FDA) dos Estados Unidos em um comunicado. O tratamento, denominado CAR-T, foi aprovado pela primeira vez em novembro de 2017 para cânceres do sangue2 potencialmente fatais. Mas a FDA afirmou que recebeu 19 relatos de novos tipos de câncer1 no sangue2 em pacientes que receberam o tratamento. Dessa forma, a agência lançou uma investigação sobre o que chamou de “risco sério” de malignidades de células3 T em pacientes tratados com terapias de células3 T com receptor de antígeno4 quimérico autólogo (CAR) visando o antígeno4 de maturação de células3 B (BCMA) ou CD19.
[Mais...]
Um pequeno ensaio clínico de um tratamento para redução do colesterol1 baseado na edição genética CRISPR produziu resultados promissores. O efeito já dura seis meses desde que o primeiro participante foi tratado, e a expectativa é que seja permanente – mas um ataque cardíaco em uma pessoa levantou preocupações de segurança. As descobertas foram apresentadas nas Sessões Científicas de 2023 da American Heart Association e relatados pela Verve Therapeutics em um comunicado. Nas três pessoas com hipercolesterolemia2 familiar heterozigótica que receberam as doses mais elevadas do VERVE-101, os níveis de colesterol1 LDL3, que está ligado ao risco de doenças cardíacas, caíram entre 39 e 55 por cento.
[Mais...]
Apenas 13 anos após a descrição da técnica de edição genética CRISPR, os órgãos reguladores do Reino Unido aprovaram o “primeiro tratamento genético do mundo” em 15 de novembro, para o tratamento da doença falciforme e da talassemia1 β dependente de transfusão2. Casgevy (exagamglogene autotemcel [exa-cel]) é o primeiro medicamento que utiliza a ferramenta de edição genética CRISPR a ser licenciado para uso em pacientes. A decisão histórica poderá transformar o tratamento da doença falciforme e da talassemia1 β, mas a tecnologia é cara.
[Mais...]
Uma forma de terapia genética estabilizou ou melhorou a retinopatia diabética1 (RD) por até um ano, particularmente em pacientes com RD não proliferativa (NP), mostrou um pequeno estudo clínico, com resultados divulgados em comunicado da REGENXBIO, publicado na Cision PR Newswire. No geral, cerca de 40% dos pacientes melhoraram o estado da doença e outros 30% apresentaram doença estável após uma única injeção2 de RGX-314 direcionado ao fator de crescimento do endotélio vascular3 (VEGF). No subgrupo de pacientes com RDNP, 29 dos 30 apresentaram doença estável ou melhora na Escala de Gravidade da Retinopatia Diabética1 (DRSS), incluindo todos os pacientes tratados com a dose mais elevada.
[Mais...]
A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou em 25/09/2023 o medicamento Mounjaro (tirzepatida), fabricado pela farmacêutica Eli Lilly. O medicamento é indicado como adjuvante à dieta e exercícios para melhorar o controle glicêmico de adultos com diabetes mellitus1 tipo 2. Em ensaios clínicos2, além de reduzir efetivamente a HbA1c3, o receptor de GIP e agonista4 do receptor GLP-1 ajudou pessoas com sobrepeso5 ou obesidade6 a perder peso significativo.
[Mais...]
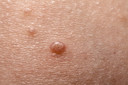
A cantaridina tópica (Ycanth) foi aprovada como o primeiro tratamento específico para o molusco contagioso1, anunciou a Food and Drug Administration (FDA) dos Estados Unidos. O novo tratamento é uma combinação de medicamento-dispositivo que contém uma formulação de solução de cantaridina (0,7%), administrada topicamente por meio de um aplicador de uso único, que permite dosagem precisa e administração direcionada. 54% dos indivíduos tratados com Ycanth atingiram a eliminação completa de todas as protuberâncias do molusco tratadas no dia 84, em comparação com 13% dos indivíduos tratados com placebo2.
[Mais...]
A Food and Drug Administration (FDA) dos Estados Unidos aprovou o inibidor do checkpoint imunológico dostarlimabe (Jemperli) mais quimioterapia1 como uma opção de primeira linha para certos pacientes com câncer2 de endométrio3 avançado ou recorrente. A aprovação foi baseada nos resultados provisórios do estudo RUBY de fase III, que mostrou que a adição de dostarlimabe à quimioterapia1 de primeira linha na população dMMR/MSI-H reduziu o risco de progressão da doença ou morte em 71% em comparação com a quimioterapia1 isolada.
[Mais...]
Uma vacina1 administrada durante a gravidez2 produziu anticorpos3 contra estreptococos do grupo B que foram transferidos para os bebês4 em limiares de IgG associados a um risco reduzido de doença invasiva por estreptococos do grupo B, mostrou um estudo randomizado5 controlado por placebo6 de fase II publicado no The New England Journal of Medicine. Entre as grávidas que receberam uma vacina1 hexavalente glicoconjugada de polissacarídeo capsular – material de reação cruzada (GBS6), foram induzidas respostas de anticorpos3 para todos os sorotipos, com proporções de anticorpos3 materno-infantil de cerca de 0,4 a 1,3, dependendo da dose recebida, resultando em concentrações associadas a um risco reduzido de doença invasiva.
[Mais...]
A Food and Drug Administration (FDA) dos Estados Unidos aprovou o brexpiprazol (Rexulti) para agitação associada à demência1 da doença de Alzheimer2. A nova indicação para o brexpiprazol o tornará o primeiro tratamento aprovado pela FDA para esta condição. O antipsicótico atípico foi aprovado anteriormente para o tratamento de transtorno depressivo maior e esquizofrenia3.
[Mais...]
|