FDA autoriza uso emergencial de plasma convalescente como tratamento potencial para a COVID-19
A U.S. Food and Drug Administration (FDA) emitiu uma autorização de uso emergencial (EUA, do inglês Emergency Use Authorization) de plasma1 convalescente experimental para o tratamento da COVID-19 em pacientes hospitalizados, como parte dos esforços da agência para combater a COVID-19. Com base nas provas científicas disponíveis, a FDA concluiu que este produto pode ser eficaz no tratamento da COVID-19 e que os benefícios potenciais conhecidos superam os riscos potenciais conhecidos do produto.
A ação de autorização segue-se à extensa revisão da ciência e dos dados gerados pela FDA ao longo dos últimos meses, resultantes dos esforços para facilitar o acesso de emergência2 ao plasma1 convalescente para os pacientes, uma vez que os ensaios clínicos3 para demonstrar definitivamente a segurança e a eficácia continuam em andamento.
A EUA autoriza a distribuição de plasma1 convalescente de COVID-19 nos EUA e a sua administração por prestadores de cuidados de saúde4, conforme apropriado, para tratar COVID-19 suspeita ou confirmada em laboratório em pacientes hospitalizados com COVID-19.
Leia sobre "Tratamento de cinco pacientes gravemente enfermos com COVID-19 com plasma1 convalescente" e "Mapeando o SARS-CoV-2".
Alex Azar, Secretário da Saúde4 e de Serviços Humanos:
"A autorização emergencial da FDA para o plasma1 convalescente é um marco importante nos esforços do Presidente Trump para salvar vidas da COVID-19", disse o Secretário Azar. "A Administração Trump reconheceu o potencial do plasma1 convalescente desde o início. Meses atrás, a FDA, a BARDA, e parceiros privados começaram a trabalhar para tornar este produto disponível em todo o país, continuando a avaliar os dados através de ensaios clínicos3. O nosso trabalho sobre o plasma1 convalescente proporcionou um acesso mais amplo ao produto do que o disponível em qualquer outro país e atingiu mais de 70.000 pacientes americanos até o momento. Estamos profundamente gratos aos americanos que já doaram e encorajamos os indivíduos que se recuperaram da COVID-19 a considerar a possibilidade de doar plasma1 convalescente".
Stephen M. Hahn, M.D., Comissário da FDA:
"Estou empenhado em liberar tratamentos seguros e potencialmente úteis para a COVID-19 o mais rapidamente possível, a fim de salvar vidas. Sentimo-nos encorajados pelos primeiros dados promissores que temos visto sobre o plasma1 convalescente. Os dados de estudos realizados este ano mostram que o plasma1 de pacientes que se recuperaram da COVID-19 tem o potencial de ajudar a tratar aqueles que sofrem os efeitos de terem contraído este terrível vírus5", disse o Dr. Hahn. "Ao mesmo tempo, continuaremos a trabalhar com pesquisadores para continuar os ensaios clínicos3 randomizados com o objetivo de estudar a segurança e eficácia do plasma1 convalescente no tratamento de pacientes infectados com o novo coronavírus".
Provas científicas sobre o Plasma1 Convalescente
Com base numa avaliação dos critérios da autorização de uso emergencial (EUA) e na totalidade das provas científicas disponíveis, o FDA’s Center for Biologics Evaluation and Research determinou que os critérios estatutários para a emissão de um critério de EUA foram cumpridos.
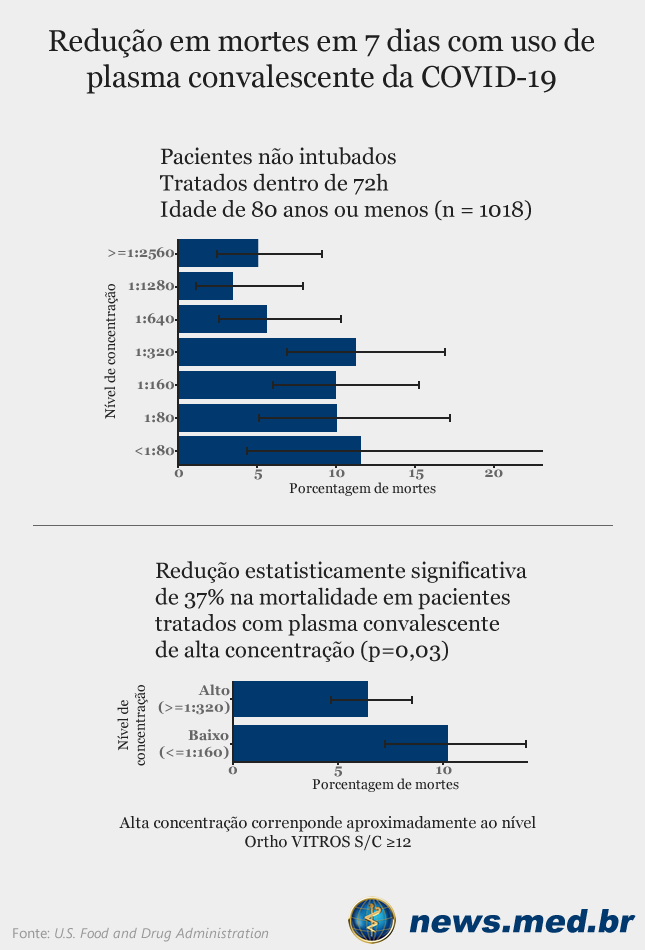
A FDA determinou que é razoável acreditar que o plasma1 convalescente da COVID-19 pode ser eficaz para diminuir a gravidade ou encurtar a duração da doença COVID-19 em alguns pacientes hospitalizados. A agência também determinou que os benefícios potenciais conhecidos do produto, quando utilizado para tratar a COVID-19, superam seus potenciais riscos conhecidos e que não existem tratamentos alternativos adequados, aprovados e disponíveis.
A EUA não se destina a substituir os ensaios clínicos3 randomizados, e facilitar a inscrição de pacientes em quaisquer dos ensaios clínicos3 randomizados em curso é extremamente importante para a demonstração definitiva da segurança e eficácia do plasma1 convalescente da COVID-19. A FDA continua a recomendar que os desenhos dos ensaios clínicos3 randomizados em curso de plasma1 convalescente da COVID-19 e de outros agentes terapêuticos permaneçam inalterados, uma vez que o plasma1 convalescente da COVID-19 ainda não representa um novo padrão de cuidados com base nas atuais provas disponíveis.
Termos da EUA
A EUA exige que as fichas de informação que fornecem importantes informações sobre a utilização do plasma1 convalescente no tratamento da COVID-19 sejam disponibilizadas aos prestadores de cuidados de saúde4 e aos pacientes, incluindo instruções de dosagem e potenciais efeitos secundários. Os possíveis efeitos secundários do plasma1 convalescente da COVID-19 incluem reações alérgicas, sobrecarga circulatória associada à transfusão6, lesões7 pulmonares associadas à transfusão6, bem como o potencial de infecções8 transmitidas por transfusão6.
Programa de Acesso Expandido da Mayo Clinic
A FDA facilitou inicialmente o acesso ao plasma1 convalescente para o tratamento da COVID-19, utilizando vias que incluíam ensaios clínicos3 tradicionais e aplicações de emergência2 em paciente único de nova droga experimental (IND, do inglês Investigational New Drug).
Um Programa de Acesso Expandido para o plasma1 convalescente foi iniciado em abril para preencher uma necessidade urgente de fornecer ao paciente acesso a um produto médico de possível benefício durante um período em que a FDA estava trabalhando com pesquisadores para facilitar o início de ensaios clínicos3 randomizados para estudar o plasma1 convalescente. Uma vez que o número de pedidos de INDs começou a chegar às centenas diariamente, a FDA trabalhou em colaboração com parceiros industriais, acadêmicos e governamentais para implementar um protocolo de acesso expandido para fornecer plasma1 convalescente a pacientes necessitados em todo o país através do protocolo nacional de tratamento de acesso expandido. O programa foi desenvolvido com financiamento da HHS’ Biomedical Advanced Research and Development Authority (BARDA), com a Mayo Clinic servindo como instituição líder. Até o momento, o programa tem facilitado a infusão de mais de 70.000 pacientes com plasma1 convalescente.
A Autorização de Uso Emergencial (EUA) foi emitida para o Escritório do HHS do Secretário Adjunto para Preparação e Resposta.
A EUA permanece em vigor até o término da declaração de que existem circunstâncias que justificam a autorização do uso emergencial de medicamentos e produtos biológicos para prevenção e tratamento da COVID-19. A EUA pode ser revisada ou revogada se for determinado que ela não atende mais aos critérios legais para emissão.
Veja também sobre "Tratamentos medicamentosos para COVID-19", "Imunidade9 de células10 T específica para SARS-CoV-2 em casos de COVID-19" e "Falha imunológica na COVID-19 grave".
Fonte: U.S. Food and Drug Administration, em 23 de agosto de 2020.