Nova técnica terapêutica contra o câncer consegue enganar um tumor para que se auto elimine
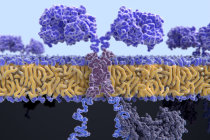
Pesquisadores da Universidade de Zurique modificaram um adenovírus respiratório comum para entrar em células1 tumorais como um cavalo de Tróia e entregar genes para uma variedade de tratamentos.
Esses genes enganam as células1 tumorais para que produzam anticorpos2 terapêuticos, fazendo com que sejam eliminadas de dentro para fora.
A abordagem futurística pode representar um grande avanço em comparação com a quimio ou radioterapia3, uma vez que não ataca as células1 saudáveis.
Os pesquisadores esperam que sua técnica, chamada SHREAD (adenovírus blindado, redirecionado [em inglês shielded, retargeted adenovírus]), possa até ajudar nas terapias relacionadas à COVID, permitindo que os genes sejam administrados diretamente aos pulmões4.
“Nós enganamos o tumor5 para que se elimine por meio da produção de agentes anticâncer por suas próprias células”, disse a pós-doutoranda da Universidade de Zurique Sheena Smith, líder de desenvolvimento, em um comunicado.
Um artigo sobre a técnica foi publicado na revista Proceedings of National Academy of Sciences.
“Os agentes terapêuticos, como anticorpos2 terapêuticos ou substâncias de sinalização, em sua maior parte ficam no local do corpo onde são necessários, em vez de se espalharem pela corrente sanguínea, onde podem danificar órgãos e tecidos saudáveis”, disse o líder do grupo de pesquisa Andreas Plückthun.
No estudo, os pesquisadores demonstram como a plataforma de terapia gênica SHREAD para entrega parácrina melhora a localização do tumor5 e os efeitos intratumorais de um anticorpo6 clínico.
Leia sobre "É possível acabar com o câncer7?", "Câncer7: o que é" e "Distinção entre tumores benignos e malignos".
Significância do estudo
Um desafio na terapia do câncer7 é fornecer níveis elevados e consistentes de terapêutica8 aos tumores. Terapêuticas baseadas em proteínas9 (por exemplo, anticorpos2) são normalmente administradas por via intravenosa e requerem várias doses para obter níveis suficientes para trafegar em tumores para exercer um efeito. No entanto, tecidos saudáveis também são expostos a níveis semelhantes de drogas, o que pode levar a efeitos colaterais10 significativos.
Este estudo usa imagens tridimensionais sofisticadas de tumores transparentes para caracterizar uma plataforma de terapia gênica versátil usando adenovírus que resolve esse problema ao produzir drogas diretamente no tumor5.
Esta abordagem aumenta em 1.800 vezes o nível tumor5-para-corrente sanguínea de um anticorpo6 modelo em comparação com a administração direta. Assim, este sistema poderia permitir a produção local de drogas altamente potentes com risco muito reduzido de toxicidades sistêmicas.
Resumo do estudo
O objetivo da administração de drogas contra o câncer7 é atingir altos níveis de terapêutica8 dentro de tumores com exposição sistêmica mínima que poderia causar toxicidade11. A produção de produtos biológicos diretamente in situ12 onde se difundem e atuam localmente é uma alternativa atraente para a administração direta de terapêuticas recombinantes, uma vez que a secreção pelo próprio tumor5 fornece altas concentrações locais que atuam de forma parácrina continuamente por um período prolongado (entrega parácrina).
Os pesquisadores projetaram uma plataforma de terapia gênica SHielded, REtargeted ADenovirus (SHREAD) que visa células1 específicas com base em marcadores de superfície escolhidos e os converte em biofábricas secretoras de terapêuticas.
Em uma prova de conceito13, um anticorpo6 clinicamente aprovado é entregue a tumores ortotópicos em um sistema modelo no qual a biodistribuição precisa pode ser determinada usando limpeza de tecido14 com a técnica CLARITY passiva (PACT) com imagem tridimensional de alta resolução e quantificação de recursos dentro dos tumores tornados transparentes.
Demonstrou-se altos níveis de transdução específica para células1 tumorais e produção significativa e durável de anticorpos2. A PACT fornece uma quantificação localizada da substância terapêutica8 secretada e permite observar diretamente a formação de poros no tumor5 e a destruição da vasculatura intacta.
A produção in situ12 do anticorpo6 levou a uma razão de concentração tumor5-para-soro15 de anticorpo6 aumentada em 1.800 vezes em comparação com a administração direta.
Essas análises bioquímicas e microscópicas detalhadas mostram, portanto, que a administração parácrina com SHREAD pode permitir o uso de combinações terapêuticas altamente potentes, incluindo aquelas com toxicidade11 sistêmica, para atingir janelas terapêuticas adequadas.
Veja também sobre "Marcadores tumorais", "Quinze sintomas16 de câncer7 que muitas mulheres ignoram" e "Câncer7 - informações importantes".
Fontes:
Proceedings of National Academy of Sciences, publicação em 25 de maio de 2021.
Neoscope, notícia publicada em 18 de maio de 2021.