Vírus do herpes que combate o câncer demonstra ser um tratamento eficaz para alguns tipos de melanoma avançado
O vírus1 herpes simplex tipo 1 (HSV-1), que afeta quase dois terços da população mundial e geralmente está associado ao herpes oral, pode causar herpes labial doloroso, com bolhas de febre2 ao redor da boca3.
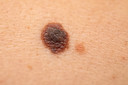
No entanto, quando geneticamente modificado para combater o câncer4, o vírus1 também pode desempenhar um papel importante no tratamento do melanoma5 avançado, um câncer4 de pele6 que se espalhou para outras partes do corpo, de acordo com os resultados de ensaios clínicos7 de fase 1-2 publicados no Journal of Clinical Oncology e recentemente apresentados pela Keck Medicine da University of Southern California (USC) na reunião anual de 2025 da Sociedade Americana de Oncologia Clínica.
O estudo envolveu 140 pacientes do ensaio clínico IGNYTE, que incluiu a Keck Medicine e outros centros em todo o mundo. Esses pacientes tinham melanoma5 avançado que não respondeu ou parou de responder à imunoterapia, que utiliza o próprio sistema imunológico8 do corpo para combater o câncer4.
Os pacientes foram tratados com um HSV-1 geneticamente modificado em combinação com uma imunoterapia (nivolumabe). Ao final do ensaio clínico, um terço dos participantes teve seus tumores reduzidos em pelo menos 30%, e em quase um de cada seis pacientes os tumores desapareceram completamente.
“Essas descobertas são muito encorajadoras porque o melanoma5 é o quinto câncer4 mais comum em adultos, e cerca de metade de todos os casos de melanoma5 avançado não podem ser tratados com os tratamentos de imunoterapia disponíveis atualmente”, disse Gino Kim In, MD, oncologista da Keck Medicine e pesquisador principal no centro de ensaios clínicos7 da Keck Medicine. O Dr. In também é membro do comitê diretor do ensaio IGNYTE e um dos principais pesquisadores do ensaio. “A taxa de sobrevivência9 do melanoma5 avançado intratável é de apenas alguns anos, então esta nova terapia oferece esperança aos pacientes que podem ter ficado sem opções para combater o câncer4.”
O HSV-1 geneticamente modificado avaliado no estudo, RP1, faz parte de uma classe relativamente nova e inovadora de medicamentos de imunoterapia contra o câncer4, conhecidos como vírus1 oncolíticos, projetados para atingir e destruir tumores cancerígenos, gerando uma resposta imune antitumoral em todo o corpo. O RP1 não causa herpes.
Saiba mais sobre "Câncer4 de pele6", "Melanoma5" e "Imunoterapia".
Em janeiro de 2025, a Food and Drug Administration (FDA) dos EUA concedeu revisão prioritária ao RP1 com nivolumabe para pacientes10 com melanoma5 avançado cujo câncer4 não havia respondido à imunoterapia anterior.
Quando injetado em um tumor11, o RP1 se replica, destruindo as células12 cancerígenas e deixando as células12 saudáveis ilesas. Além disso, o RP1 estimula os glóbulos brancos do corpo a procurar e destruir quaisquer outras células12 cancerígenas no corpo.
O segundo medicamento contra o câncer4 usado no estudo, o nivolumabe, é um tratamento de imunoterapia padrão no combate ao melanoma5 avançado e outros tipos de câncer4 que se espalharam pelo corpo. Os pesquisadores teorizaram que o nivolumabe, que funciona usando o próprio sistema imunológico8 do corpo para combater e destruir células12 cancerígenas, aumentaria o efeito potencial do RP1.
Os pacientes admitidos no estudo já haviam sido tratados com sucesso mínimo por uma ou mais terapias de imunoterapia e precisavam ter mais de um tumor11 que pudesse ser injetado com RP1. Alguns tumores foram considerados “superficiais”, ou seja, visíveis na pele6 ou logo abaixo dela, e alguns estavam localizados em regiões mais profundas do corpo, como no fígado13 ou nos pulmões14. Os pesquisadores injetaram RP1 em tumores superficiais e profundos.
Durante o ensaio clínico, os pacientes receberam uma terapia combinada15 de RP1 e nivolumabe a cada duas semanas por até oito ciclos. Se os pacientes respondessem ao tratamento, continuavam com nivolumabe isolado a cada quatro semanas por até 30 ciclos (ou dois anos).
Os pesquisadores mediram tanto os tumores tratados quanto os não tratados. Eles descobriram que não apenas o tamanho do tumor11 injetado diminuiu 30% em um terço dos pacientes, mas que os tumores não injetados dos pacientes também diminuíram ou até desapareceram, com a mesma frequência e profundidade.
“Este resultado sugere que o RP1 é eficaz no combate ao câncer4 em todo o corpo e não apenas no tumor11 injetado, o que amplia a eficácia potencial do medicamento, visto que alguns tumores podem ser mais difíceis ou impossíveis de atingir”, disse o Dr. In.
O estudo também constatou que o RP1 foi bem tolerado e apresentou um resultado de segurança favorável.
Embora seja muito cedo para dizer se os resultados positivos permanecerão permanentes, o Dr. In está otimista quanto ao futuro da terapia com RP1. “Acredito que os vírus1 oncolíticos abrirão uma nova abordagem importante para o combate ao câncer4 em alguns pacientes em um futuro próximo”, disse ele.
A fase 1-2 do ensaio clínico IGNYTE examinou a segurança, os efeitos colaterais16, a melhor dosagem e a eficácia da administração de RP1 juntamente com nivolumabe em uma população limitada de pacientes. O Dr. In e seus colegas pesquisadores lançaram agora o estudo de fase 3, conhecido como IGNYTE-3, para confirmar suas descobertas em uma população global de mais de 400 participantes.
Confira a seguir o resumo do artigo publicado.
Leia sobre "Herpes Simples - o que é" e "5 passos para proteger a pele6 contra o câncer4".
RP1 combinado com nivolumabe em melanoma5 avançado com falha anti-PD-1 (IGNYTE)
As opções eficazes de tratamento para melanoma5 após falha do bloqueio do ponto de controle imunológico são limitadas. O RP1 (vusolimogene oderparepvec) é uma imunoterapia oncolítica baseada em HSV-1, aqui avaliada em combinação com nivolumabe em melanoma5 com falha anti-PD-1.
Os pacientes apresentavam melanoma5 avançado com progressão confirmada em anti-PD-1 (≥8 semanas, último tratamento anterior). O RP1 foi administrado por via intratumoral (≤8 doses, ≤10 mL/dose; doses adicionais permitidas) com nivolumabe (≤2 anos). A taxa de resposta objetiva (TRO) foi avaliada por revisão central independente utilizando os Critérios de Avaliação de Resposta em Tumores Sólidos versão 1.1.
Dos 140 pacientes incluídos, 48,6% apresentavam doença em estágio IV M1b/c/d, 65,7% apresentavam resistência primária anti-PD-1, 56,4% eram PD-L1 negativos e 46,4% receberam terapia anti-PD-1 e anti-CTLA-4 anteriormente (43,6% em combinação e 2,9% sequencialmente).
A TRO confirmada (IC 95%) foi de 32,9% (25,2%-41,3%; 15,0% de resposta completa). As respostas ocorreram com frequência, profundidade, duração e cinética17 semelhantes para lesões18 injetadas e não injetadas, incluindo lesões18 viscerais. A duração mediana (IC 95%) da resposta foi de 33,7 meses (14,1-não atingida).
As taxas de sobrevida19 global (IC 95%) em 1 e 2 anos foram de 75,3% (66,9%-81,9%) e 63,3% (53,6%-71,5%), respectivamente.
A análise de biomarcadores demonstrou ampla ativação imunológica associada à resposta, incluindo aumento da infiltração de células12 T CD8+ e da expressão de PD-L1. As taxas de eventos adversos relacionados ao tratamento foram de 77,1% grau 1/2, 9,3% grau 3, 3,6% grau 4 e nenhum evento grau 5.
O estudo concluiu que o RP1 combinado com nivolumabe proporcionou respostas sistêmicas profundas e duradouras em pacientes com melanoma5 sem sucesso no tratamento anti-PD-1, incluindo aqueles com fatores prognósticos desfavoráveis. O perfil de segurança foi favorável, com eventos adversos predominantemente grau 1/2.
Fontes:
Journal of Clinical Oncology, publicação em 08 de julho de 2025.
Keck Medicine of USC, notícia publicada em 08 de julho de 2025.