Primeiro tratamento de VSR para bebês e crianças foi aprovado nos EUA
A Food and Drug Administration (FDA) dos EUA aprovou o primeiro tratamento para prevenir infecções1 graves pelo vírus2 sincicial respiratório (VSR) em crianças e bebês3.
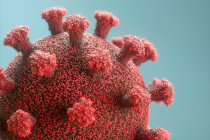
O VSR é um vírus2 comum que circula no outono e no inverno. A maioria das crianças com VSR geralmente apresenta sintomas4 leves de resfriado, mas algumas – especialmente aquelas expostas ao vírus2 pela primeira vez – podem desenvolver doenças respiratórias com risco de vida, como pneumonia5 e bronquiolite. Bebês3 prematuros e aqueles com doença pulmonar crônica da prematuridade ou doença cardíaca congênita6 significativa correm maior risco de doença grave por VSR.
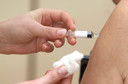
O tratamento, chamado Beyfortus (nirsevimabe), é uma dose única administrada por injeção7 antes ou durante a primeira temporada de VSR do bebê. Crianças de até 2 anos que permanecem vulneráveis ao VSR durante sua segunda temporada de VSR, como aquelas com doença pulmonar ou cardíaca crônicas, também são elegíveis para a injeção7.
Saiba mais sobre "O que são vírus2", "Doenças respiratórias" e "Resfriado comum: como é".
Aproximadamente 1 a 3 por cento das crianças menores de 1 ano são hospitalizadas por VSR a cada ano nos EUA, de acordo com a FDA. No ano passado, houve uma temporada notavelmente ruim de VSR, já que os hospitais de todo o país lutavam para acompanhar o aumento de casos, o que causou escassez de medicamentos.
“O VSR pode causar doenças graves em bebês3 e algumas crianças e resulta em um grande número de atendimentos de emergência8 e em consultórios médicos a cada ano”, disse John Farley, do Centro de Avaliação e Pesquisa de Medicamentos da FDA, em um comunicado. “A aprovação de hoje atende à grande necessidade de produtos para ajudar a reduzir o impacto da doença por VSR em crianças, famílias e o sistema de saúde9.”
Beyfortus, fabricado pela empresa farmacêutica AstraZeneca, não é uma vacina10. Em vez disso, usa anticorpos11 monoclonais contra o VSR. Estas são proteínas12 projetadas para imitar os anticorpos11 produzidos pelo sistema imunológico13 para afastar patógenos nocivos. Ao contrário de uma vacina10, o tratamento não treina o corpo para identificar o VSR ou produzir seus próprios anticorpos11 em resposta à infecção14. Os efeitos colaterais15 incluem erupção16 cutânea17 e dor, inchaço18 ou vermelhidão no local da injeção7.
A FDA tomou sua decisão com base em dados de três ensaios clínicos19 (Ensaios 03, 04 e 05), que incluíram quase 4.000 bebês3. Nesses ensaios, uma única dose de Beyfortus reduziu o risco de bebês3 precisarem de cuidados médicos para uma infecção14 por VSR entre 70 e 75 por cento.
O principal parâmetro de eficácia foi a incidência20 de infecção14 do trato respiratório inferior por VSR com atendimento médico (ITRI VSR AM), avaliada durante os 150 dias após a administração de Beyfortus. ITRI VSR AM incluiu todas as consultas com um prestador de cuidados de saúde9 (consultório médico, atendimento de urgência21, atendimentos de emergência8 e hospitalização) para doença do trato respiratório inferior com agravamento da gravidade clínica e um teste de VSR positivo. Os ensaios 03 e 04 foram ensaios clínicos19 randomizados, duplo-cegos, controlados por placebo22 e multicêntricos.
O ensaio 03 incluiu 1.453 bebês3 prematuros (nascidos com idade gestacional maior ou igual a 29 semanas até menos de 35 semanas de gestação) que nasceram durante ou entrando em sua primeira temporada de VSR. Dos 1.453 bebês3 prematuros no estudo, 969 receberam uma dose única de Beyfortus e 484 receberam placebo22. Entre as crianças que foram tratadas com Beyfortus, 25 (2,6%) apresentaram ITRI VSR AM em comparação com 46 (9,5%) crianças que receberam placebo22. Beyfortus reduziu o risco de ITRI VSR AM em aproximadamente 70% em relação ao placebo22.
Para o ensaio 04, o grupo de análise primária dentro do ensaio incluiu 1.490 bebês3 nascidos a termo e prematuros tardios (nascidos com idade gestacional maior ou igual a 35 semanas), 994 dos quais receberam uma dose única de Beyfortus e 496 dos quais receberam placebo22. Entre as crianças que foram tratadas com Beyfortus, 12 (1,2%) apresentaram ITRI VSR AM em comparação com 25 (5,0%) crianças que receberam placebo22. Beyfortus reduziu o risco de ITRI VSR AM em aproximadamente 75% em relação ao placebo22.
O estudo 05, um estudo multicêntrico randomizado23, duplo-cego, controlado por ativo (palivizumabe), apoiou o uso de Beyfortus em crianças de até 24 meses de idade que permanecem vulneráveis à doença grave por VSR durante a segunda temporada de VSR. O estudo inscreveu 925 bebês3 prematuros e bebês3 com doença pulmonar crônica da prematuridade ou doença cardíaca congênita6. Os dados de segurança e farmacocinética do ensaio 05 forneceram evidências para o uso de Beyfortus para prevenir ITRI VSR AM nesta população.
Beyfortus não deve ser administrado a bebês3 e crianças com histórico de reações graves de hipersensibilidade aos ingredientes ativos de Beyfortus ou a qualquer um de seus excipientes.
Beyfortus vem com advertências e precauções sobre reações graves de hipersensibilidade, incluindo anafilaxia24, que foram observadas com outros anticorpos11 monoclonais IgG1 humanos. Beyfortus deve ser administrado com cautela a lactentes25 e crianças com distúrbios hemorrágicos26 clinicamente significativos.
No início deste ano, a FDA aprovou duas vacinas contra o VSR para idosos. No final deste ano, a agência também deve decidir sobre uma vacina10 materna contra o VSR, que protegeria os recém-nascidos da doença.
Leia sobre "Pneumonia5 na infância" e "Bronquiolite em bebês3 e crianças pequenas".
Fontes:
Food and Drug Administration, publicação em 17 de julho de 2023.
New Scientist, notícia publicada em 17 de julho de 2023.