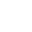Antibiótico ‘inteligente’ pode matar bactérias mortais enquanto poupa o microbioma
Patógenos classificados como bactérias Gram-negativas são frequentemente resistentes, virulentos e rápidos em desenvolver resistência a antibióticos. Apenas alguns medicamentos podem eliminá-los, e estes medicamentos também destroem bactérias intestinais benéficas.
Agora, pesquisadores desenvolveram o composto chamado lolamicina, que tem como alvo um grupo de micróbios nocivos, mas não perturba aqueles que vivem pacificamente no intestino.
O novo antibiótico reduziu ou eliminou infecções1 bacterianas resistentes a medicamentos em modelos de camundongo com pneumonia2 aguda e sepse3, poupando micróbios saudáveis no intestino do camundongo. O medicamento também evitou infecções1 secundárias com Clostridioides difficile, uma infecção4 bacteriana comum e perigosa associada a hospitais, e foi eficaz contra mais de 130 cepas5 bacterianas multirresistentes em cultura de células6.
As descobertas foram detalhadas na revista Nature.
“As pessoas estão começando a perceber que os antibióticos que todos nós tomamos — que estão combatendo infecções1 e, em alguns casos, salvando nossas vidas — também estão tendo esses efeitos deletérios sobre nós”, disse o professor de química da Universidade de Illinois em Urbana-Champaign, Paul Hergenrother, que liderou o estudo com a ex-aluna de doutorado Kristen Muñoz. “Eles estão matando nossas bactérias boas enquanto tratam a infecção4. Queríamos começar a pensar sobre a próxima geração de antibióticos que poderiam ser desenvolvidos para matar as bactérias patogênicas e não as benéficas.”
Vários estudos descobriram que distúrbios relacionados a antibióticos no microbioma7 intestinal aumentam a vulnerabilidade a novas infecções1 e estão associados a problemas gastrointestinais, renais, hepáticos e outros.
“A maioria dos antibióticos clinicamente aprovados mata apenas bactérias Gram-positivas ou matam ambas bactérias Gram-positivas e Gram-negativas”, disse Muñoz.
Saiba mais sobre "Bactérias Gram-positivas e Gram-negativas" e "Resistência aos antibióticos".
Bactérias Gram-positivas e Gram-negativas diferem na composição de suas paredes celulares. Bactérias Gram-negativas têm uma camada dupla de proteção, tornando-as mais difíceis de matar, disse Muñoz.
Os poucos medicamentos disponíveis para combater infecções1 Gram-negativas também matam outras bactérias Gram-negativas potencialmente benéficas. Por exemplo, a colistina, um dos poucos antibióticos somente Gram-negativos aprovados para uso clínico, pode causar diarreia8 associada a C. difficile e colite9 pseudomembranosa, uma complicação potencialmente fatal. O medicamento também tem efeitos tóxicos no fígado10 e nos rins11 e “portanto, a colistina é normalmente utilizada apenas como um antibiótico de último recurso”, escreveram os pesquisadores.
Para lidar com os muitos problemas associados ao direcionamento indiscriminado de bactérias Gram-negativas, a equipe se concentrou em um conjunto de medicamentos desenvolvidos pela empresa farmacêutica AstraZeneca. Esses medicamentos inibem o sistema Lol, um sistema de transporte de lipoproteínas exclusivo de bactérias Gram-negativas e geneticamente diferente em micróbios patogênicos e benéficos. Esses medicamentos não eram eficazes contra infecções1 Gram-negativas, a menos que os pesquisadores primeiro minassem as principais defesas bacterianas em laboratório. Mas como esses antibióticos pareciam discriminar entre bactérias Gram-negativas benéficas e patogênicas em experimentos de cultura de células6, eles eram candidatos promissores para exploração posterior, disse Hergenrother.
Em uma série de experimentos, Muñoz projetou variações estruturais dos inibidores de Lol e avaliou seu potencial para combater bactérias Gram-negativas e Gram-positivas em cultura de células6. Um dos novos compostos, a lolamicina, tinha como alvo seletivo algumas “cepas laboratoriais de patógenos Gram-negativos, incluindo Escherichia coli, Klebsiella pneumoniae e Enterobacter cloacae”, descobriram os pesquisadores. A lolamicina não teve efeito detectável em bactérias Gram-positivas em cultura de células6. Em doses mais altas, a lolamicina matou até 90% dos isolados clínicos multirresistentes de E. coli, K. pneumoniae e E. cloacae.
Quando administrada oralmente a camundongos com septicemia12 ou pneumonia2 resistente a medicamentos, a lolamicina resgatou 100% dos camundongos com septicemia12 e 70% dos camundongos com pneumonia2, relatou a equipe.
Um trabalho extensivo foi feito para determinar o efeito da lolamicina no microbioma7 intestinal.
“O microbioma7 do camundongo é uma boa ferramenta para modelar infecções1 humanas porque os microbiomas intestinais humanos e de camundongos são muito semelhantes”, disse Muñoz. “Estudos mostraram que antibióticos que causam disbiose intestinal13 em camundongos têm um efeito semelhante em humanos.”
O tratamento com antibióticos padrão amoxicilina e clindamicina causou mudanças drásticas na estrutura geral das populações bacterianas no intestino do camundongo, diminuindo a abundância de vários grupos microbianos benéficos, descobriu a equipe.
“Em contraste, a lolamicina não causou nenhuma mudança drástica na composição taxonômica ao longo do tratamento de três dias ou da recuperação de 28 dias seguintes”, escreveram os pesquisadores.
Muitos mais anos de pesquisa são necessários para estender as descobertas, disse Hergenrother. Lolamicina, ou outros compostos semelhantes, devem ser testados contra mais cepas5 bacterianas e estudos toxicológicos detalhados devem ser conduzidos. Quaisquer novos antibióticos também devem ser avaliados para determinar a rapidez com que induzem resistência aos medicamentos, um problema que surge mais cedo ou mais tarde em bactérias tratadas com antibióticos.
O estudo é uma prova de conceito14 de que antibióticos que matam um micróbio patogênico15 enquanto poupam bactérias benéficas no intestino podem ser desenvolvidos para infecções1 Gram-negativas — algumas das infecções1 mais desafiadoras de tratar, disse Hergenrother.
Leia sobre "Microbioma7 intestinal humano" e "Bactérias do bem - o que elas têm a nos oferecer".
Confira a seguir o resumo do artigo publicado.
Um antibiótico seletivo para patógenos Gram-negativos que poupa o microbioma7 intestinal
As infecções1 causadas por patógenos Gram-negativos são cada vez mais prevalentes e são tipicamente tratadas com antibióticos de amplo espectro, resultando na perturbação do microbioma7 intestinal e suscetibilidade a infecções1 secundárias. Há uma necessidade crítica de antibióticos que sejam seletivos tanto para bactérias Gram-negativas em relação às bactérias Gram-positivas, quanto para bactérias patogênicas em relação às bactérias comensais.
Neste estudo, relatou-se o design e a descoberta da lolamicina, um antibiótico específico para patógenos Gram-negativos que tem como alvo o sistema de transporte de lipoproteínas. A lolamicina tem atividade contra um painel de mais de 130 isolados clínicos multirresistentes, mostra eficácia em vários modelos de camundongos de pneumonia2 aguda e infecção4 septicêmica e poupa o microbioma7 intestinal em camundongos, prevenindo infecção4 secundária com Clostridioides difficile.
A morte seletiva de bactérias Gram-negativas patogênicas pela lolamicina é uma consequência da baixa homologia de sequência para o alvo em bactérias patogênicas versus comensais; essa estratégia duplamente seletiva pode servir de modelo para o desenvolvimento de outros antibióticos que poupem o microbioma7.
Veja também sobre "Usos e abusos dos antibióticos" e "Os benefícios dos probióticos16".
Fontes:
Nature, publicação em 29 de maio de 2024.
Science Daily, notícia publicada em 29 de maio de 2024.