Laboratório de inteligência artificial alega ter resolvido “o problema de dobramento de proteínas”: descoberta poderia acelerar o desenvolvimento de medicamentos
Alguns cientistas passam a vida tentando identificar a forma de pequenas proteínas1 no corpo humano2.
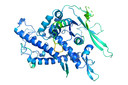
As proteínas1 são os mecanismos microscópicos3 que conduzem o comportamento de vírus4, bactérias, o corpo humano2 e todos os seres vivos. Elas começam como cadeias de compostos químicos, antes de se torcerem e se dobrarem em formas tridimensionais que definem o que elas podem fazer – e o que não podem.
Para os biólogos, identificar a forma precisa de uma proteína geralmente requer meses, anos ou mesmo décadas de experimentação. Requer habilidade e inteligência, e às vezes eles nunca têm sucesso.
Agora, um laboratório de inteligência artificial em Londres construiu um sistema de computador que pode fazer o trabalho em algumas horas – talvez até alguns minutos.
Esta descoberta pode acelerar a capacidade de compreender doenças, desenvolver novos medicamentos e desvendar mistérios do corpo humano2.
Leia sobre "O que são vírus4", "O que são bactérias" e "Papel dos alimentos ricos em proteínas1".
DeepMind, um laboratório pertencente à mesma empresa controladora do Google, disse que seu sistema, chamado AlphaFold, resolveu o que é conhecido como “o problema de dobramento de proteínas”, uma tarefa que atormenta os cientistas há mais de 50 anos. Dada a cadeia de aminoácidos que compõem uma proteína, o sistema pode prever de forma rápida e confiável sua forma tridimensional.
O sistema de inteligência artificial (IA) desenvolvido pelo laboratório atingiu assim o objetivo há muito buscado de prever com precisão a forma das proteínas1 apenas a partir de sua sequência, uma parte fundamental para compreender como funciona a máquina da vida. Em uma competição, AlphaFold foi capaz de igualar dois terços dos resultados alcançados por humanos fazendo experimentos de laboratório caros e demorados.
“Fiquei muito impressionado quando vi isso”, disse John Moult, da Universidade de Maryland, um dos organizadores da competição. “Esta é a primeira vez que chegamos perto de nos aproximar da utilidade experimental, o que é bastante extraordinário.”
As proteínas1 são vitais para a vida. As células5 estão cheias de máquinas – desde turbinas que geram energia até transportadores que andam por trilhos puxando cargas – que são construídas a partir de proteínas1, e os formatos dessas máquinas são cruciais. Por exemplo, o coronavírus pode entrar e infectar células5 porque a proteína spike em sua superfície se encaixa em um receptor nas células5 humanas, como uma chave em uma fechadura.
Essas formas dependem da sequência de 20 aminoácidos diferentes que são encadeados para formar as proteínas1. É fácil descobrir a sequência de qualquer proteína porque isso é determinado pelo DNA que a codifica. Mas, apesar de meio século de esforços, os biólogos não tinham sido capazes de descobrir a forma de uma proteína apenas a partir de sua sequência.
Em vez disso, eles tiveram que confiar em métodos experimentais, como cristalografia de raios-X, que envolve a análise do padrão de difração formado quando um feixe de raios-X é disparado através de um cristal de proteína.
“Isso é excepcionalmente difícil”, diz John Jumper, que lidera a equipe AlphaFold na DeepMind. Fazer cristais de algumas proteínas1 é difícil e interpretar os padrões de difração pode ser complicado.
A computação de força bruta baseada apenas na física não é uma opção, porque as proteínas1 são muito complexas. Em vez disso, muitos grupos em todo o mundo recorreram ao aprendizado de máquina, em que os sistemas de inteligência artificial são treinados usando conjuntos de dados de estruturas de proteínas1 conhecidas.
Para cada proteína alvo, grupos incluindo o DeepMind procuram variantes encontradas em espécies relacionadas e alimentam sua sequência e estrutura no sistema de IA, junto com a sequência da proteína alvo. A ideia é que o sistema aprenda a trabalhar a forma da proteína-alvo observando os padrões que ligam sequência e estrutura.
Em 1994, Moult e um colega criaram a competição CASP (Avaliação Crítica da Predição da Estrutura da Proteína) para julgar o desempenho das previsões do computador. Qualquer grupo que queira entrar recebe as sequências de proteínas1 cuja estrutura foi determinada experimentalmente, mas ainda não publicada.
As formas previstas são pontuadas em uma escala de 100 pontos com base em quão próximo cada aminoácido está da posição determinada pelo experimento. Uma pontuação acima de 90 é considerada equivalente aos resultados obtidos por experimentos.
Na competição de 2016, a melhor equipe obteve uma pontuação mediana em torno de 40 na categoria mais difícil. Em 2018, a primeira versão do AlphaFold obteve uma pontuação média de quase 60 nesta categoria. Este ano, um AlphaFold redesenhado obteve uma pontuação média de 87 na categoria mais difícil. Em todas as categorias, pontuou acima de 90 para dois terços das proteínas1.
Embora este resultado seja surpreendente, houve algumas falhas evidentes, diz Moult. Por exemplo, AlphaFold não se saiu bem com uma proteína cuja estrutura é influenciada por interações com outras proteínas1 que a rodeiam.
Essa variabilidade pode ser um problema, mas AlphaFold também fornece uma medida de quão confiáveis são suas previsões, para que os cientistas saibam em quais confiar, diz Jumper. “Isso é algo grandioso.”
Se os métodos do DeepMind pudessem ser refinados, Moult e outros pesquisadores disseram, eles poderiam acelerar o desenvolvimento de novos medicamentos, bem como os esforços para aplicar os medicamentos existentes a novos vírus4 e doenças.
A descoberta chega tarde demais para causar um impacto significativo no coronavírus. Mas os pesquisadores acreditam que os métodos da DeepMind podem acelerar a resposta a futuras pandemias. Alguns acreditam que também pode ajudar os cientistas a compreender melhor as doenças genéticas, como o mal de Alzheimer6 ou a fibrose cística7.
Separado da competição, Andrei Lupas, do Instituto Max Planck de Biologia do Desenvolvimento, na Alemanha, vinha tentando descobrir a estrutura de uma proteína específica por uma década até que o DeepMind se ofereceu para ajudar. Alguns ajustes foram necessários para melhorar a precisão, mas a equipe de Lupas tinha a estrutura final meia hora após receber a previsão de AlphaFold. “É surpreendente”, diz ele. “É realmente surpreendente.”
Lupas acredita que nos próximos anos os pesquisadores ainda precisarão fazer algum trabalho experimental para verificar as previsões de forma, mas eventualmente poderão contar apenas com a computação. Isso fará uma enorme diferença, diz ele, mas a verdadeira revolução virá da capacidade de usar computadores para prever como as proteínas1 interagem com outras moléculas.
“Isso vai mudar completamente a cara da medicina”, diz Lupas. Por exemplo, o AlphaFold foi capaz de prever as formas de várias proteínas1 do coronavírus logo depois que o vírus4 foi sequenciado pela primeira vez em janeiro, diz ele. Melhor ainda seria ter a capacidade de prever quais dos milhares de medicamentos existentes se ligam a essas proteínas1 e podem ter um efeito terapêutico, sem ter que fazer experimentos caros.
DeepMind revelou poucos detalhes sobre AlphaFold até agora, mas diz que em breve publicará um artigo. A empresa não soube dizer como os cientistas terão acesso à tecnologia, mas afirma que deseja que ela esteja amplamente disponível. “Queremos ter certeza de que isso tem o maior impacto”, diz Pushmeet Kohli da DeepMind.
Veja também sobre "Como o coronavírus entra no tecido8 respiratório e explora as defesas" e "Coronavírus - como é o vírus4".
Fontes:
New Scientist, notícia publicada em 30 de novembro de 2020.
The New York Times, notícia publicada em 30 de novembro de 2020.