Novo medicamento para tratar psoríase em placas é aprovado pela FDA
O Cosentyx (secukinumabe) foi aprovado pela Food and Drug Administration (FDA), dos Estados Unidos, para o tratamento de adultos com psoríase1 em placas2 moderada a grave.
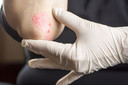
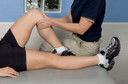
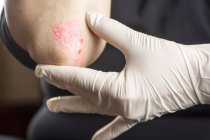
A psoríase1 é uma doença auto-imune3, crônica e não contagiosa4. A psoríase1 em placas2 é uma forma comum da doença e apresenta placas2 secas, avermelhadas com escamas prateadas ou esbranquiçadas. Essas placas2 coçam e algumas vezes doem, podendo atingir todas as partes do corpo, inclusive as regiões genitais e a mucosa5 da boca6. Em casos graves, a pele7 em torno das articulações8 pode rachar e sangrar.
A substância ativa do Cosentyx é o secukinumabe. Secukinumabe é um anticorpo9 que se liga a uma proteína que está envolvida na inflamação10, a interleucina 17 A (IL-17A). Ao ligar-se à IL-17A, o secukinumabe a impede de se ligar ao seu receptor e inibe a sua capacidade para desencadear resposta inflamatória, que desempenha um papel importante no desenvolvimento das placas2 de psoríase1.
O Cosentyx é administrado por uma injeção11 sob a pele7. Ele é destinado a pacientes que são candidatos à terapia sistêmica (tratamento com substâncias que agem através da corrente sanguínea depois de serem tomadas por via oral ou injetável), fototerapia (tratamento com luz ultravioleta) ou uma combinação de ambos.
A segurança e eficácia do Cosentyx foram estabelecidas em quatro ensaios clínicos12 com um total de 2.403 participantes com psoríase1 em placas2 que eram candidatos à fototerapia ou à terapia sistêmica. Os participantes foram aleatoriamente designados para receber Cosentyx ou placebo13. Cosentyx mostrou maior resposta clínica do que o placebo13, deixando a pele7 limpa ou quase clara, como avaliado pela pontuação da dimensão, natureza e gravidade das alterações psoriáticas da pele7.
Cosentyx está sendo aprovado com um alerta para informar aos pacientes que, por ser um medicamento que afeta o sistema imunológico14, os pacientes podem apresentar maior risco de contrair uma infecção15. Reações alérgicas graves foram relatadas com o uso de Cosentyx. Devem ser tomadas precauções quando se considera o uso desta nova medicação em pacientes com infecção15 crônica ou história de infecção15 recorrente e em pacientes com doença de Crohn16 ativa. Os efeitos colaterais17 mais comuns incluem diarreia18 e infecções19 respiratórias superiores.
Cosentyx é comercializado pela Novartis Pharmaceuticals Corporation, em East Hanover, New Jersey.