Psoríase: FDA aprova o ustekinumab, novo medicamento para a psoríase em placas
O Food and Drug Administration (FDA) aprovou um novo medicamento para o tratamento da psoríase1 em placas2, o Stelara (ustekinumab). A nova medicação é um produto biológico para uso em adultos com psoríase1 moderada ou severa.
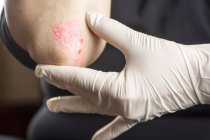
A psoríase1 em placas2 é uma doença do sistema imunológico3 que resulta em produção rápida de células4 da pele5. Ela é caracterizada pelo surgimento de lesões6 avermelhadas e descamativas, bem limitadas e de evolução crônica.
Stelara é um anticorpo7 monoclonal produzido em laboratório que mimetiza o trabalho dos anticorpos8 produzidos naturalmente pelo sistema imunológico3. O medicamento trata a psoríase1 bloqueando a ação de duas proteínas9 que contribuem para o aumento na produção de células4 da pele5 e para a inflamação10.
Três estudos com 2.266 pacientes avaliaram a segurança e a efetividade do medicamento.
Uma vez que o Stelara reduz a habilidade do sistema imune11 lutar contra infecções12, há um risco maior de desenvolver infecções12. Algumas infecções12 sérias foram relatadas em pacientes em uso do novo medicamento, por vezes ligando-as à necessidade de hospitalização. Estas infecções12 podem ser causadas por fungos, vírus13 ou bactérias que se espalharam pelo corpo. Também pode haver um risco maior de desenvolver câncer14.
O FDA está exigindo uma avaliação de risco e estratégia de atenuação para o Stelara que inclui um plano de comunicação direcionado a profissionais de saúde15 e uma orientação sobre o medicamento aos pacientes.
Fonte: FDA