Ingredientes ativos do filtro solar são absorvidos sistemicamente pelo corpo e se acumulam em altos níveis no plasma sanguíneo
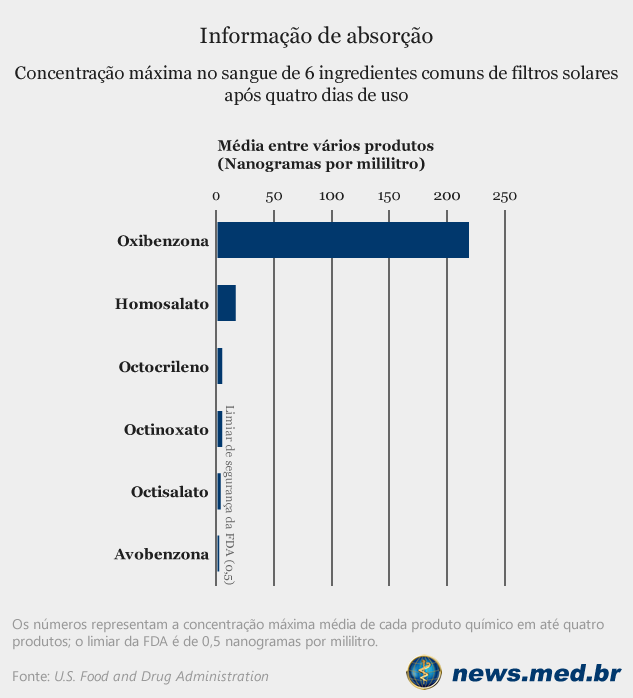
Estudo de ingredientes comuns de filtros solares estabeleceu que os produtos químicos são absorvidos na corrente sanguínea em concentrações muito superiores ao limiar de segurança da Food and Drug Administration (FDA).
Segundo a FDA, se os ingredientes ativos forem encontrados no sangue1 a um nível de 0,5 nanogramas por mililitro ou mais, eles devem ser analisados para determinar se aumentam o risco de câncer2, defeitos congênitos3 ou outros efeitos adversos.
Estudos anteriores indicaram uma possível associação entre alguns dos produtos químicos e os riscos à saúde4, como perturbações endócrinas e danos à reprodução5, mas não existem dados abrangentes sobre segurança.
Uma regra proposta pela FDA, que deveria ser finalizada em novembro passado, exigiria que a indústria concluísse testes adicionais de até uma dúzia de produtos químicos para garantir a segurança dos filtros solares. Mas a proposta foi arquivada em março, quando o presidente Trump assinou a Lei de Ajuda, Alívio e Segurança Econômica devido ao Coronavírus.
Um estudo piloto anterior, também realizado pela FDA e publicado em maio de 2019, já havia demonstrado a absorção sistêmica de 4 ingredientes ativos de filtros solares; estabelecendo a necessidade de estudos adicionais para determinar a absorção sistêmica de ingredientes ativos adicionais e a rapidez com que a exposição sistêmica excede 0,5 ng/mL.
Saiba mais sobre "Protetor solar ou filtro solar" e "Cuidados com a pele6".
Em janeiro desse ano (2020), a FDA publicou no Journal of the American Medical Association (JAMA) seu estudo mais recente sobre essa questão. Esse estudo descreve os resultados de um ensaio clínico avaliando a absorção pela pele6 e no corpo de seis ingredientes ativos de filtro solar sob dose única e condições de uso máximo.
O objetivo do estudo foi avaliar a absorção sistêmica e a farmacocinética dos 6 ingredientes ativos (avobenzona, oxibenzona, octocrileno, homosalato, octisalato e octinoxato) em 4 produtos de filtro solar em condições de uso único e máximo.
O ensaio clínico randomizado7 foi realizado em 48 participantes saudáveis em uma unidade de farmacologia8 clínica (West Bend, Wisconsin). O estudo foi realizado entre janeiro e fevereiro de 2019.
Os participantes foram randomizados para 1 de 4 produtos de filtro solar, formulados como loção (n = 12), spray em aerossol (n = 12), spray não-aerossol (n = 12) e spray de bomba (n = 12). O filtro solar foi aplicado em 2 mg/cm² em 75% da área da superfície corporal às 0 horas no dia 1 e 4 vezes do dia 2 até o dia 4 em intervalos de 2 horas, e 34 amostras de sangue1 foram coletadas ao longo de 21 dias de cada participante.
O desfecho primário foi a concentração plasmática máxima de avobenzona nos dias 1 a 21. Os desfechos secundários foram as concentrações plasmáticas máximas de oxibenzona, octocrileno, homosalato, octisalato e octinoxato nos dias 1 a 21.
Entre 48 participantes randomizados (idade média [DP], 38,7 [13,2] anos; 24 mulheres [50%]; 23 brancos [48%], 23 afro-americanos [48%], 1 asiática [2%] e 1 raça/etnia desconhecida [2%]), 44 (92%) completaram o estudo.
As médias geométricas das concentrações plasmáticas máximas de todos os 6 ingredientes ativos foram superiores a 0,5 ng/mL, e esse limite foi ultrapassado no dia 1 após uma única aplicação para todos os ingredientes ativos.
Para a avobenzona, as concentrações plasmáticas máximas totais foram de 7,1 ng/mL (coeficiente de variação [CV], 73,9%) para loção; 3,5 ng/mL (CV, 70,9%) para spray em aerossol; 3,5 ng/mL (CV, 73,0% ) para spray não-aerossol e 3,3 ng/mL (CV, 47,8%) para spray de bomba.
Para a oxibenzona, as concentrações foram de 258,1 ng/mL (CV, 53,0%) para loção e 180,1 ng/mL (CV, 57,3%) para spray em aerossol.
Para octocrileno, as concentrações foram 7,8 ng/mL (CV, 87,1%) para loção, 6,6 ng/mL (CV, 78,1%) para spray em aerossol e 6,6 ng/mL (CV, 103,9%) para spray não-aerossol.
Para o homosalato, as concentrações foram de 23,1 ng/mL (CV, 68,0%) para spray em aerossol, 17,9 ng/mL (CV, 61,7%) para spray não-aerossol e 13,9 ng/mL (CV, 70,2%) para spray de bomba.
Para o octisalato, as concentrações foram de 5,1 ng/mL (CV, 81,6%) para spray em aerossol, 5,8 ng/mL (CV, 77,4%) para spray não-aerossol e 4,6 ng/mL (CV, 97,6%) para spray de bomba.
Para octinoxato, as concentrações foram de 7,9 ng/mL (CV, 86,5%) para spray não-aerossol e 5,2 ng/mL (CV, 68,2%) para spray de bomba.
O evento adverso mais comum foi erupção9 cutânea10, que se desenvolveu em 14 participantes.
Neste estudo realizado em uma unidade de farmacologia8 clínica e examinando11 a aplicação de filtro solar entre participantes saudáveis, todos os 6 dos ingredientes ativos testados administrados em 4 formulações diferentes de filtro solar foram absorvidos sistemicamente e tinham concentrações plasmáticas que excederam o limiar da FDA para potencialmente renunciar a alguns dos estudos adicionais de segurança para protetores solares. Esses achados não indicam que os indivíduos devem abster-se do uso de filtro solar.
Leia sobre "Queimadura de sol ou eritema12 solar" e "Câncer2 de pele6".
Fontes:
JAMA, estudo publicado em 21 de janeiro de 2020.
FDA, comunicado publicado em 21 de janeiro de 2020.
The Wall Street Journal, notícia publicada em 17 de julho de 2020.