FDA aprova Eucrisa para tratar o eczema
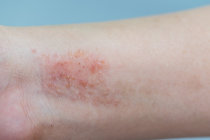
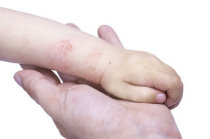
A dermatite1 atópica, uma doença inflamatória crônica da pele2, é muitas vezes referida como "eczema3", que é um termo geral usado para classificar vários tipos de inflamação4 da pele2. A dermatite1 atópica é o mais comum de muitos tipos de eczema3, tendo início geralmente na infância e podendo durar até a idade adulta.
A causa da dermatite1 atópica é uma combinação de fatores genéticos, imunes e ambientais. A pele2 fica avermelhada, com escamas e crostas extremamente pruriginosas5. Podem ocorrer edemas6, rachaduras, eliminação de líquidos claros e espessamento da pele2.
Saiba mais sobre a "Dermatite1 atópica".
A aprovação da pomada Eucrisa (crisaborole) oferece outra opção de tratamento para pacientes7 que tratam de dermatite1 atópica leve a moderada, segundo Amy Egan, vice-diretora do Office of Drug Evaluation III no FDA’s Center for Drug Evaluation and Research (CDER).
A Eucrisa pode ser aplicada topicamente, duas vezes por dia. Ela é um inibidor da fosfodiesterase 4 (PDE-4), embora seu mecanismo específico de ação na dermatite1 atópica ainda não seja conhecido.
A segurança e a eficácia de Eucrisa foram estabelecidas em dois ensaios controlados por placebo8, com um total de 1.522 participantes, com idades entre 2 e 79 anos de idade, com dermatite1 atópica leve a moderada. Em geral, os participantes que receberam Eucrisa obtiveram maior resposta com pele2 curada ou quase curada após 28 dias de tratamento.
Os efeitos secundários graves de Eucrisa incluem reações de hipersensibilidade. Eucrisa não deve ser utilizada em doentes que tenham tido uma reação de hipersensibilidade ao ingrediente ativo crisaborole. O efeito colateral9 mais comum de Eucrisa é a dor no local de aplicação, incluindo ardor10 ou sensação de picadas.
A Eucrisa é fabricada pela Anacor Pharmaceuticals, Inc., com sede em Palo Alto, Califórnia.
Leia também sobre a "Dermatite Seborreica11".