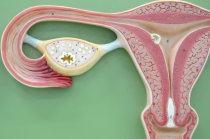
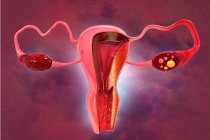
Novo estudo investigou como os óvulos humanos permanecem frescos por décadas
Nos seres humanos, os óvulos precisam sobreviver por cerca de cinco décadas, muito mais do que a maioria dos outros tipos de células1, e podem atingir essa vida útil excepcionalmente longa desacelerando seus processos celulares naturais.
Um estudo publicado no periódico científico The EMBO Journal mostra que os óvulos humanos parecem eliminar seus resíduos mais lentamente do que outras células1, o que pode ajudá-los a evitar o desgaste e explicar por que vivem mais.
Toda mulher nasce com um número finito de óvulos, ou ovócitos, que precisam sobreviver por cerca de cinco décadas. Para as células1, esse é um tempo anormalmente longo. Embora algumas células1 humanas, como as do cérebro2 e dos olhos3, possam viver tanto quanto você, a maioria tem uma vida útil muito mais curta, em parte porque os processos naturais que permitem seu funcionamento também as danificam com o tempo.
As células1 precisam reciclar suas proteínas4 como uma forma de manutenção necessária, mas isso tem um custo. A energia consumida nesse processo pode gerar moléculas chamadas espécies reativas de oxigênio, ou EROs, que causam danos aleatórios na célula5. “Esse dano acontece em segundo plano o tempo todo”, diz Elvan Böke, do Centro de Regulação Genômica da Espanha. “Quanto mais EROs houver, maior será o dano.”
Leia sobre "Alguns conceitos ligados à reprodução6 humana", "Infertilidade7 feminina" e "Climatério8 e menopausa9: como são".
Mas óvulos saudáveis parecem evitar esse problema. Para descobrir o porquê, Böke e seus colegas estudaram óvulos humanos coletados sob um microscópio. As células1 foram colocadas em um líquido com corantes fluorescentes, que se ligam a componentes celulares ácidos, chamados lisossomos, que se comportam como “usinas de reciclagem”, diz Gabriele Zaffagnini, da Universidade de Colônia, na Alemanha.
O corante brilhante revelou que os lisossomos de descarte de resíduos em óvulos humanos eram menos ativos do que os mesmos componentes em outros tipos de células1 humanas ou aqueles em óvulos de mamíferos menores, como camundongos. Zaffagnini e seus colegas afirmam que isso pode ser uma forma de autopreservação.
Desacelerar seu mecanismo de descarte de resíduos pode ser apenas uma das muitas maneiras pelas quais os óvulos humanos alcançam sua vida útil relativamente longa, diz Zaffagnini. Böke especula que, para evitar danos, os ovócitos humanos “travam tudo”. Se todos os processos celulares ocorrerem mais lentamente em óvulos humanos, diz ela, isso poderia resultar em níveis mais baixos de EROs prejudiciais e, portanto, menos risco de danos.
Como atrasar o processo de reciclagem de proteínas4 parece ajudar os óvulos a manterem sua saúde10, não fazê-lo pode explicar o que torna alguns ovócitos doentes. “Na minha opinião, isso pode ser uma pista sobre por que os ovócitos humanos realmente se tornam disfuncionais11 após um certo tempo”, diz Emre Seli, da Faculdade de Medicina de Yale. “Pode ser uma transição para uma avaliação avançada de tudo o que dá errado nos ovócitos humanos”, afirma.
Avaliar a saúde10 dos óvulos dessa forma pode, eventualmente, aprimorar os tratamentos de fertilidade. “Sabemos que a degradação de proteínas4 é essencial para a sobrevivência12 celular, portanto, afeta 100% a fertilidade”, diz Böke. Ela observa que o estudo se concentrou em óvulos saudáveis, e que o trabalho para comparar essas células1 com óvulos de pessoas afetadas por complicações de fertilidade está em andamento. “Se houver alto teor de EROs na célula5, os resultados da fertilização13 in vitro são ruins”, afirma.
Os óvulos humanos ainda não são bem compreendidos, pois são difíceis de estudar. “Eles são difíceis de trabalhar, porque a limitação da amostra é um problema”, diz Böke. Seli afirma que esse obstáculo é uma das “múltiplas camadas” do problema, que também incluem regulamentações que restringem o estudo de óvulos e a falta de financiamento.
Se esses obstáculos puderem ser superados, diz Zaffagnini, pode haver resultados “realmente surpreendentes”. “Vale muito a pena”, afirma.
Veja também sobre "Ciclo menstrual", "Indutores da ovulação14" e "Ovulação14: entenda o fenômeno da arborização".
No artigo publicado, os pesquisadores relatam o panorama proteostático de ovócitos humanos saudáveis.
Eles contextualizam que os ovócitos, células germinativas15 femininas que se desenvolvem em óvulos, estão entre as células1 com maior longevidade no corpo animal. Estudos recentes com ovócitos de camundongos destacam adaptações únicas na homeostase proteica (proteostase) dentro dessas células1. No entanto, os mecanismos de proteostase em ovócitos humanos permanecem praticamente inexplorados.
Apresentou-se então o primeiro estudo em larga escala da atividade proteostática em ovócitos humanos utilizando mais de 100 ovócitos recém-doados de 21 mulheres saudáveis com idades entre 19 e 34 anos. Analisou-se a atividade e a distribuição de lisossomos, proteassomas e mitocôndrias16 em ovócitos imaturos e maduros.
Notavelmente, os ovócitos humanos apresentam atividade proteolítica quase duas vezes menor do que as células somáticas17 circundantes, com reduções adicionais à medida que os ovócitos amadurecem. A maturação dos ovócitos também está associada à exocitose18 lisossomal e à diminuição do potencial de membrana mitocondrial.
Propõe-se que a atividade reduzida de organelas preserva componentes celulares essenciais para o desenvolvimento embrionário inicial durante a maturação prolongada de ovócitos humanos.
Essas descobertas destacam a biologia distinta dos ovócitos humanos e a necessidade de investigar a biologia reprodutiva específica de humanos para enfrentar os desafios da fertilidade feminina.
Fontes:
The EMBO Journal, publicação em 16 de julho de 2025.
New Scientist, notícia publicada em 16 de julho de 2025.